Possiamo considerare due tipologie di ipertrofia.
Un primo tipo di ipertrofia, che potremmo definire "ipertrofia transitoria", consiste nel gonfiore che interessa i distretti muscolari impegnati in un lavoro (ad esempio, l’allenamento con i sovraccarichi), durante il lavoro stesso. Questo aumento di volume è, però, solo temporaneo in quanto causato da uno spostamento di fluidi dal comparto plasmatico al ventre muscolare interessato. Qualche minuto dopo il termine dell'allenamento, le dimensioni del muscolo ritorneranno ad essere le stesse che aveva precedentemente, se non minori, in quanto nel muscolo saranno presenti meno glicogeno (usato per fornire energia all'allenamento) e meno acqua, che era ad esso legata.
Il secondo tipo di ipertrofia, quello generalmente ricercato da chi si allena con i sovraccarichi, prende il nome "ipertrofia cronica", ed è uno degli adattamenti che il corpo mette in atto in risposta all'allenamento con i sovraccarichi. Questo tipo di ipertrofia non avviene durante l'allenamento, ma nelle ore (e nei giorni) seguenti lo stimolo allenante, ed è più duraturo nel tempo.
Quando un evento turba lo stato di equilibrio del nostro corpo (stato di omeostasi), il nostro corpo cerca di costruire delle difese per fare in modo che, se l'evento si dovesse ripresentare in futuro, il suo stato di equilibrio non venga nuovamente turbato, o perlomeno, venga turbato di meno.
L'ipertrofia è una delle difese (adattamenti) che il nostro corpo mette in atto quando è stato stressato dalla richiesta di un lavoro muscolare eccessivo rispetto alle sue possibilità.
L’aumento delle dimensioni del muscolo è la risultante di diverse concause:
L’ipertrofia della fibra muscolare, a sua volta, è data dall’aumento quantitativo di tutte le componenti della fibra, in particolare:
Ognuno degli adattamenti sopracitati è il risultato della risposta della fibra muscolare ad uno specifico stimolo.
Con il termine iperplasia si intende l’aumento del numero di cellule muscolari.
La possibilità del verificarsi dell’iperplasia nel tessuto muscolare nell’uomo è un’argomentazione controversa ed è stata a lungo dibattuta in quanto le fibre muscolari, originando dalla fusione di cellule precursori, i mioblasti, non hanno capacità mitotica.
Studi effettuati su animali hanno, però, dimostrato la possibilità del verificarsi dell’iperplasia e sulla sua origine si sono prodotte diverse teorie.
Attualmente è accreditata l’ipotesi che l’iperplasia nel muscolo scheletrico non sia data dalla “riproduzione" per mitosi delle cellule esistenti, ma da un processo che chiama in causa le cellule satelliti, ovvero cellule precursori delle cellule muscolari, non ancora “fuse" ad altre cellule.
Le cellule satellite, cellule precursori delle fibre muscolari, non fuse alle fibre adulte, risiedono nelle vicinanze delle cellule muscolari completamente formate, tra il sarcolemma e la lamina basale e, proprio perché non sono fuse ad altre cellule, hanno conservato la loro capacità mitotica.
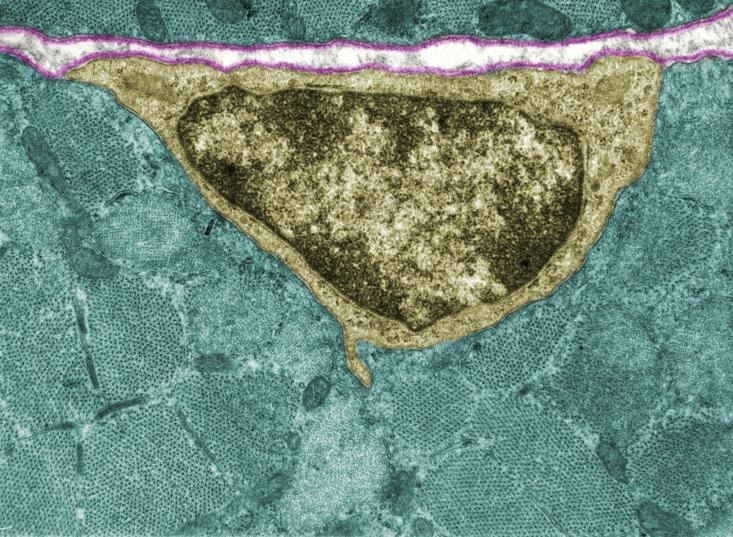
Figura 1: Immagine di una cellula satellite localizzata tra il sarcolemma e la lamina basale.
Normalmente le cellule satelliti sono in stato inattivo (quiescente) ma, in presenza di uno stimolo adatto, come, ad esempio, un danno muscolare, vengono attivate.
Una volta attivate queste si riproducono e hanno due possibilità, fondersi alle fibre muscolari esistenti (ipertrofia) o allinearsi tra loro e formare una nuova fibra muscolare ex novo (iperplasia).
Il ruolo delle cellule satellite diviene fondamentale non solo per spiegare il meccanismo dell’iperplasia, ma anche per il realizzarsi dell’ipertrofia, infatti, fondendosi alla fibra danneggiata, la cellula satellite le “dona" il suo nucleo, incrementando così il numero di nuclei della fibra matura e, quindi, la sua capacità di sintetizzare nuove proteine contrattili.
Questa ipotesi viene confermata anche dal principio del “dominio dei mionuclei", secondo il quale i nuclei delle fibre muscolari sono in grado di regolare la produzione di mRNA, e quindi sintesi proteica, solo per una quantità finita di sarcoplasma ed ogni incremento delle dimensioni della fibra deve, quindi, essere accompagnato da un aumento del numero di mionuclei.
L’attuale ipotesi sull’ipertrofia indica che questa sarebbe il risultato dalla sommatoria di due fattori, un aumento del numero di domini dei mionuclei, dato dall’incremento del numero di nuclei donati dalle cellule satellite, e un aumento delle dimensioni dei domini stessi.
Le cellule satellite, inoltre, secernono, come le fibre muscolari adulte, vari fattori di regolazione che regolano la riparazione, la rigenerazione e la crescita del tessuto muscolare.
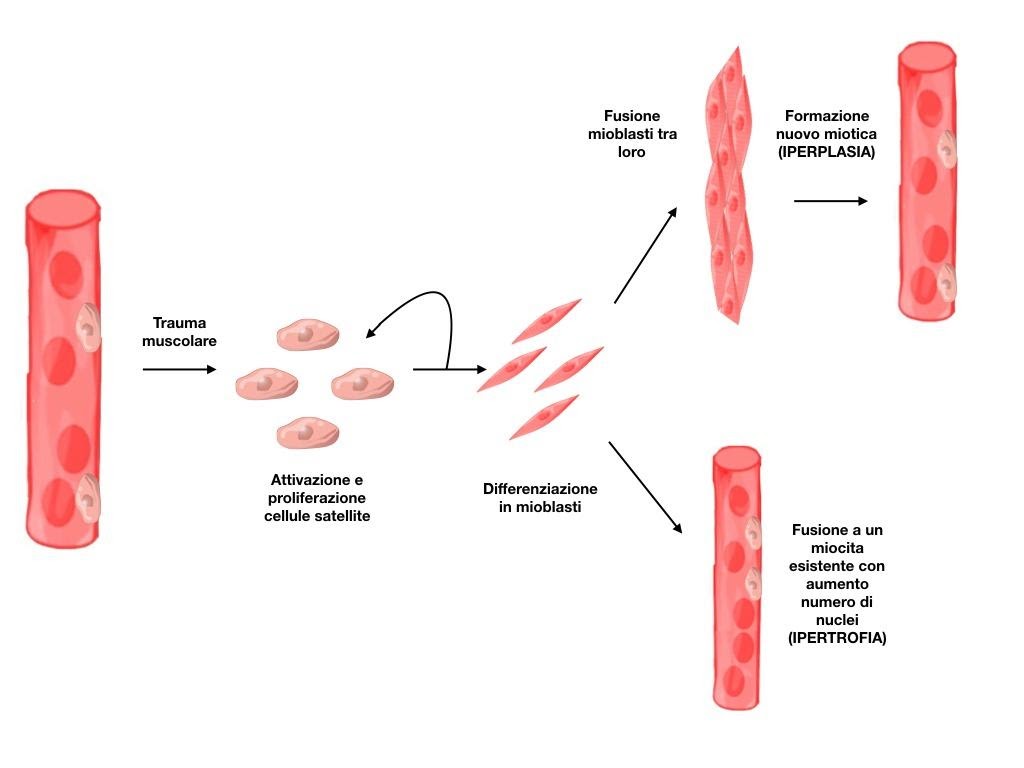
Figura 2: apporto delle cellule satellite all'ipertrofia ed all'iperplasia. Durante la crescita e la rigenerazione muscolare, le cellule satellite si riproducono per mitosi dando origine a cellule precursori mono-nucleati delle fibre muscolari, i mioblasti, i quali vengono attivati e si fondono l'uno con l'altro per generare nascenti miotubi o si fondono con i miotubi esistenti, incrementandone il numero di nuclei, favorendo la sintesi proteica.
L'allenamento è in grado di indurre ipertrofia attraverso l'induzione di diverse tipologie di stress al muscolo interessato, che possiamo riassumere come:
La tensione meccanica è il più importante dei fattori che inducono ipertrofia in seguito all'allenamento con i sovraccarichi. La tensione esercitata sulla fibra muscolare stimola alcune proteine che fungono da recettori di tensione. Una volta attivate, queste proteine, avviano una cascata di eventi intracellulari che induce sintesi proteica e inibisce il catabolismo, inducendo, conseguentemente, ipertrofia.
Sono varie le proteine funzionanti come sensori di tensione, le principali sembrano essere le integrine, un gruppo di proteine della famiglia dei costameri (proteine di adesione), che oltre a connettere il citoscheletro alla matrice extracellulare fungono, appunto, da sensori di tensione, attivando, in seguito alla loro attivazione, la principale proteina che regola positivamente la sintesi proteica, mTor.
Figura 3: le integrine
Una seconda proteina che funge da sensore di tensione è la titina, che ha la funzione di fissare le molecole di miosina alle linee Z nel sarcomero. La titina contiene una porzione elastica che, quando attivata, attiva dei secondi messaggeri che non sembrano direttamente correlati a mTor, ma piuttosto attraverso il complesso Murf1/2-Proteosoma.
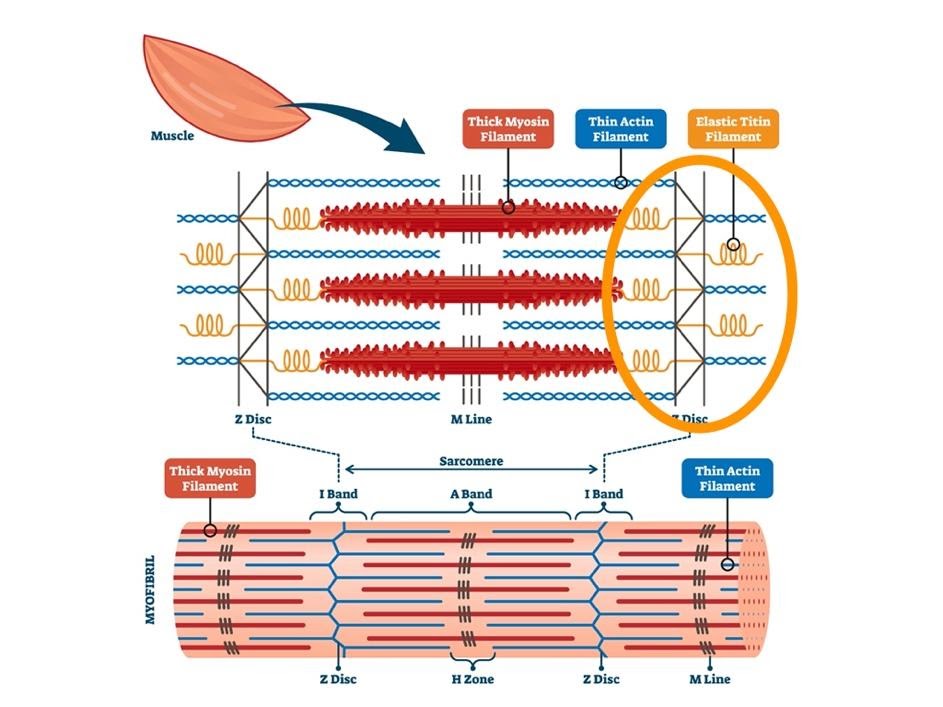
Figura 4: La titina
Anche la FIlamina-C e Bag-3 , due proteine localizzate nel disco Z, fungono da recettori di tensione attivando, quando stimolate, varie vie enzimatiche legate alla sintesi proteica: mTor, la cascata di segnalazione intracellulare Hippo e l’autofagia selettiva.
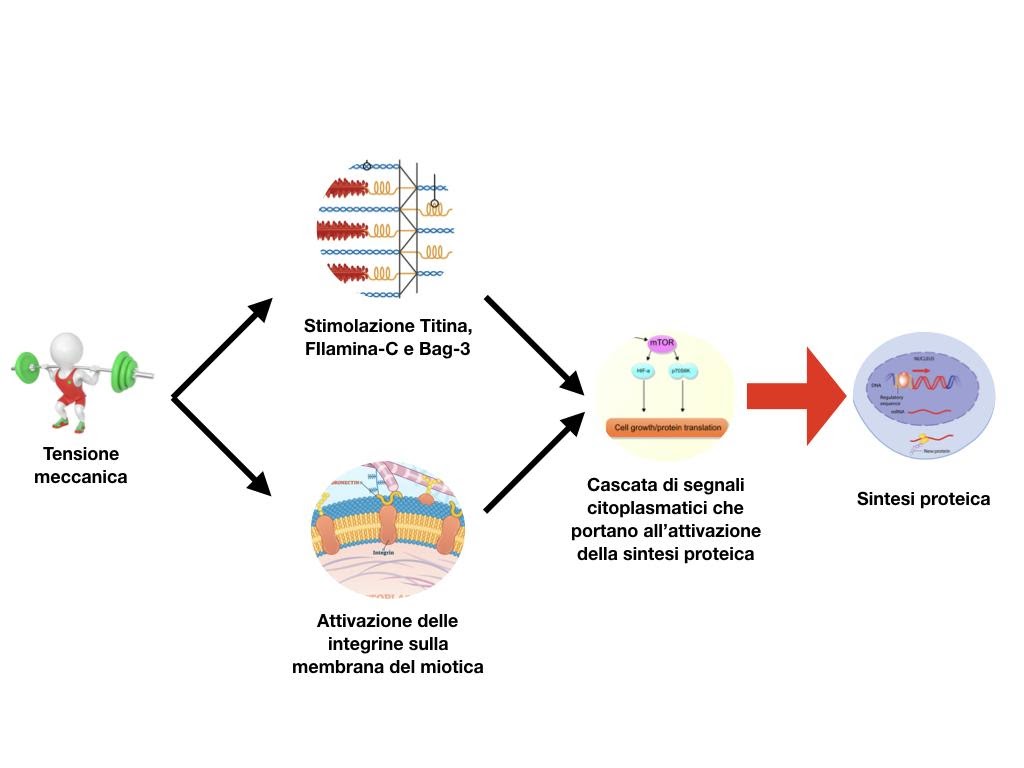
Figura 5: Lo stimolo meccanico
Per stress metabolico si intende l'accumulo dei metaboliti prodotto dal sovra utilizzo dei sistemi energetici, in particolare anaerobico lattacido, dovuto all'allenamento con i sovraccarichi (lattato, fosfati inorganici ed ioni H+). Lo stress metabolico, attraverso le seguenti vie, è in grado di innescare i meccanismi ipertrofici:
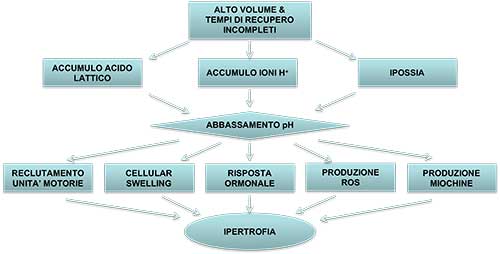
Figura 6: Stress metabolico ed ipertrofia. Modificato da: Schoenfeld, B. (2016). Science and development of muscle hypertrophy. Human Kinetics
L'esercizio con sovraccarico, in particolare l’allungamento, il sovraccarico eccentrico ed il lavoro ad ampio range di movimento, induce lesioni alla microstruttura della fibra muscolare. Tali microlesioni sono, generalmente, seguite da infiammazione locale, disturbi nella regolazione del calcio, catabolismo e presenza, nel sangue, di proteine plasmatiche muscolari.
Non è ancora chiaro se, ed in quale misura, il danno muscolare indotto da esercizio, sia importante al fine dell’ipertrofia muscolare, anche per la difficoltà nel distinguere, durante i lavori di ricerca, gli affetti dovuti alle lesioni e quelli dovuti agli altri fattori.
I diversi autori hanno constatato che è possibile ipertrofia anche in assenza di danno muscolare e l’insufficienza del solo danno muscolare ad indurre ipertrofia. Si è concluso, quindi, che il danno muscolare sia associato ad ipertrofia ma si devono ancora capire i meccanismi che stanno alla base della risposta.
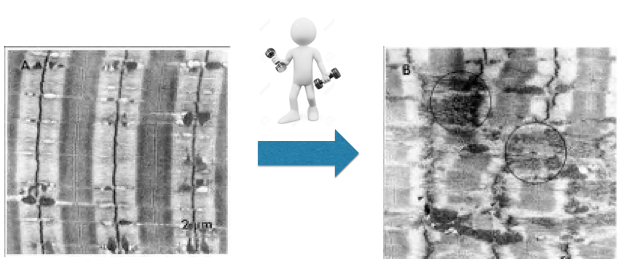
Figura 7: le microlesioni
L'esercizio con sovraccarico, in misura diversa dipendentemente dal volume e dall'intensità dei carichi utilizzati, è in grado di stimolare maggiormente l'una o l'altra delle vie presentate ed indurre, quindi, ipertrofia.
Lo stimolo meccanico sarà maggiore quando l’entità dei carichi utilizzati sarà maggiore, quindi con l’uso di carichi più vicini al massimale, con la conseguente esecuzione di un basso numero di ripetizioni e mantenendo i tempi di recupero tra le serie completi (> di 2’30" -3’) al fine di riuscire, di serie in serie, ad utilizzare nuovamente carichi elevati.
I protocolli che portano alla massimizzazione dello stress metabolico, invece, sono quelli che prevedono un massiccio utilizzo del metabolismo anaerobico lattacido: questo si verifica quando si eseguono serie di allenamento con carichi sub-massimali (65% dell’1RM) protratte fino al temporaneo cedimento (circa 15-20 ripetizioni), con tempi di recupero incompleti tra le serie (durata inferiore a 2 minuti) e volumi di lavoro alti.
Le microlesioni sono una conseguenza dell’uso di sovraccarichi che può avvenire con entrambe le tipologie di stimolazione, in particolare se si enfatizza la fase eccentrica del movimento.
Nella pratica del bodybuilding rivolto ad atleti avanzati, al fine di incrementare ulteriormente l’entità dello stimolo allenante dell’uno o dell’altro tipo, vengono utilizzate, oltre alle metodiche di allenamento per l’ipertrofia descritte in precedenza, anche tecniche particolari di allenamento, denominate tecniche di intensità.
Nel programmare il lavoro per l’ipertrofia si alterneranno, quindi, dei periodi di lavoro destinati all'incremento della forza massimale, nei quali si utilizzeranno carichi superiori all'85% del massimale e si manterranno tempi di recupero completi tra le serie (circa 3'), a periodi di lavoro direttamente rivolti all'ipertrofia nei quali si utilizzeranno carichi compresi tra il 70 e l'85% del massimale, che consentano di eseguire un numero di ripetizioni compreso tra le 8 e le 12/15 e quindi di indurre un buon livello di stress metabolico senza ridurre eccessivamente anche lo stimolo meccanico.
I fattori chiave comprendono intensità, volume, recupero e stimolazione ormonale.
L'allenamento di resistenza causa microlesioni che attivano processi di riparazione e adattamento.
La nutrizione fornisce i nutrienti essenziali per la sintesi proteica e il recupero muscolare.
L'articolo esamina i meccanismi fisiologici e le strategie per l'ipertrofia muscolare, integrando l'importanza dell'allenamento, della nutrizione e del recupero. Vengono analizzati i processi adattativi e le metodologie per massimizzare la crescita muscolare in modo efficace e sicuro, evidenziando un approccio integrato per risultati ottimi.